توضیحات
اسید بنزوئیک چیست و چه کاربردی دارد؟
اسید بنزوئیک benzoic acid یک ترکیب بلوری بیرنگ (سفید دیده میشود) است. اسید بنزوییک سادهترین کربوکسیلیک اسید آروماتیک نیز میباشد.این ماده یک اسید ضعیف بهشمار میرود. از نمکهای آن به عنوان نگهدارندههای غذایی استفاده میشود، همچنین در ساخت بسیاری از ترکیبات آلی دیگر از این ماده استفاده میشود. ضمناً این ترکیب از تمشک و توت فرنگی به دست می آید.
اسید بنزوئیک چیست
بنزوئیک اسید یک ترکیب آلی جامد سفید (یا بی رنگ) با فرمول C6H5COOH است که ساختار آن از یک حلقه بنزن (C6H6) با یک جایگزین کربوکسیل (-C(=O)OH) تشکیل شده است. گروه بنزوئیل اغلب به اختصار “Bz” خوانده می شود (نباید با “Bn” که برای بنزیل استفاده می شود اشتباه گرفته شود)، بنابراین اسید بنزوئیک نیز به عنوان BzOH نشان داده می شود، زیرا گروه بنزوئیل دارای فرمول -C6H5CO است.
این ساده ترین اسید کربوکسیلیک معطر است. این نام از صمغ بنزوئین گرفته شده است که برای مدت طولانی تنها منبع آن بود. اسید بنزوئیک به طور طبیعی در بسیاری از گیاهان وجود دارد و به عنوان یک واسطه در بیوسنتز بسیاری از متابولیت های ثانویه عمل می کند.
نمک بنزوئیک اسید به عنوان نگهدارنده مواد غذایی استفاده می شود. بنزوئیک اسید یک پیش ساز مهم برای سنتز صنعتی بسیاری از مواد آلی دیگر است. نمک ها و استرهای بنزوئیک اسید به نام بنزوات شناخته می شوند.1).
بنزوئیک اسید در قرن شانزدهم میلادی کشف شد. اولین بار شخصی به نام نوستراداموس از تقطیر خشک مادهای سنتی به نام gum benzoin بدست آورد.
در سال ۱۸۷۵ شخصی به نام سالکوفسکی نیز پی به خواص ضد قارچ بنزوئیک اسید برد.
تولید اسید بنزوئیک
از نظر صنعتی، اسید بنزوئیک را می توان با استفاده از گاز اکسیژن برای اکسیداسیون جزئی تولوئن تهیه کرد. می توان اشاره کرد که در این فرآیند معمولا از نفتنات منگنز یا کبالت به عنوان کاتالیزور استفاده می شود. این ترکیب را می توان از طریق هیدرولیز بنزامید و بنزونیتریل نیز تهیه کرد. همچنین می توان آن را با اکسید کردن بنزیل کلرید یا بنزیل الکل یا هر مشتق دیگری از گروه بنزیل تهیه کرد.2.)
یکی از روشهای تجاری ساخت اسید بنزوئیک، اکسایش جزئی تولوئن با گاز اکسیژن در مجاورت کاتالیزور کبالت یا منگنز نفتنات است که با بازدهٔ بالا و رعایت اصول محیط زیستی (شیمی سبز) انجام میشود که تصویر واکنش مربوطه را در زیر میبینید:
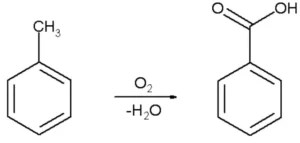
بنزوئیک اسید، مادهٔ ارزان قیمت و در دسترسی است، در نتیجه در صورت نیاز به آن لازم نیست زحمت سنتز آن را متقبل شویم و فقط کافی است نمونهٔ تجاری آن را خریداری کرده و متناسب با کارمان آن را خالص سازی کنیم. برای اینکار استفاده از روش دیگری به نام تبلور مجدد با دو حلال با حلالهای اتانول و آب بسیار مناسب میباشد. ولی در هر صورت میتوان آن را به روشهای زیر نیز سنتز کرد:
با هیدرولیز: از هیدرولیز بنزونیتریل، بنزآمید در محیطهای اسیدی یا بازی شدید میتوان بنزوئیک اسید یا آنیون آن را بدست آورد.
بنزالدهید: همچنین میتوان با استفاده از واکنش کانیزارو ی تقاطعی بنزوئیک اسید را از بنزالدهید ساخت که واکنش مربوط به آن را در زیر میبینید:
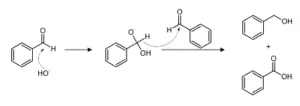
همچنین میتوان از اکسایش بنزیل الکل در حضور محلول پتاسیم پرمنگنات داغ نیز استفاده کرد. در این روش بلافاصله بعد از واکنش باید محلول در حالت داغ فیلتر شود تا منگنز دیاکسید تشکیل شده جدا شود و سپس محلول به حال خود رها میشود تا بلورهای بنزوئیک اسید تشکیل شود.
کاربرد اسید بنزوئیک
در محیط های صنعتی، بنزوئیک اسید بیشترین کاربرد را برای تولید طیف وسیعی از محصولات مانند عطر، رنگ، داروهای موضعی و دافع حشرات دارد. نمک اسید بنزوئیک (بنزوات سدیم) به طور گسترده ای به عنوان تنظیم کننده pH مواد غذایی و نگهدارنده استفاده می شود و از رشد میکروب ها برای حفظ سلامت غذا جلوگیری می کند.
اسید بنزوئیک به جلوگیری از ایجاد عفونت توسط باکتری ها کمک می کند. بدن توسط اسید سالیسیلیک کمک می کند تا سلول های زبر یا مرده پوست را از بین ببرد. دارویی که برای درمان تحریک و التهاب پوست ناشی از سوختگی، نیش حشرات، عفونت های قارچی یا اگزما استفاده می شود، اسید بنزوئیک و اسید سالیسیلیک موضعی (برای پوست) است.
اسید بنزوئیک به جلوگیری از ایجاد عفونت توسط باکتری ها کمک می کند. بدن توسط اسید سالیسیلیک کمک می کند تا سلول های زبر یا مرده پوست را از بین ببرد. دارویی که برای درمان تحریک و التهاب پوست ناشی از سوختگی، نیش حشرات، عفونت های قارچی یا اگزما استفاده می شود، اسید بنزوئیک و اسید سالیسیلیک موضعی (برای پوست) است.3.)
کاربردهای صنعتی
برای تهیهٔ بنزیل کلرید: بنزوئیل کلرید را می توان با واکنش تیونیل کلرید یا پنتاکلرید فسفر با بنزوئیک اسید تهیه کرد. اسید بنزوئیک خشک در یک فلاسک، در نهایت پنتا کلرید فسفر پودر شده، تصفیه می شود.4).
برای تهیهٔ فنول: فنول (C۶H۵OH) از کربوکسیل زدایی همراه با اکسایش در دمای ۳۰۰oC الی ۴۰۰oC بدست میآید. البته این فرایند میتواند در حضور کاتالیزور نمک کبالت در ۲۰۰oC هم انجام پذیرد. فنول (Phenol) نیز استفادههای بسیاری دارد، که مهمترین آنها تبدیل فنول به سیکلوهگزانول میباشد که سرآغازی برای تولید نایلون است.
مشخص است که فنل را می توان از بنزوئیک اسید با تصفیه بنزوئیک اسید مذاب با گاز اکسید کننده، ترجیحاً هوا، و بخار در ZOO-250 C بدست آورد. نمک مس محلول در اسید مذاب به عنوان کاتالیزور استفاده می شود.5).
در صنایع غذایی
اسید بنزوئیک و نمکهایش به عنوان نگهدارندهٔ غذا مصرف دارند که به نامهای E212, E۲۱۱، E۲۱۰ و E۲۱۳ شناخته میشوند. هر کدام از این نمکها از واکنش مستقیم یا واکنش با نمکهای سدیم، پتاسیم یا کلسیم تهیه میشوند. در اصل این ماده از رشد قارچها، مخمرها و بعضی باکتریها جلوگیری میکند.
نحوهٔ اثر بنزوئیک اسید اینگونه است که در ابتدا این ماده جذب سلول میشود، اگر pH درون سلولی به ۵ یا کمتر تغییر کند، تخمیر ناهوازی گلوکز از طریق Phosphofructokinase به میزان ۹۵٪ کاهش مییابد و این خود باعث نابودی آنها میشود. مقدار معمول استفاده از بنزوئیک اسید و نمکهایش به عنوان نگه دارنده بین ۰٫۰۵٪-۰٫۱٪ میباشد.
البته در بعضی غذاها باید از سطوح بالاتری از بنزوئیک اسید استفاده شود که مقادیر ماکسیمم آن در قوانین بینالمللی غذا موجود است. البته نگرانیهایی وجود دارد مبنی بر اینکه بنزوئیک اسید با آسکوربیک اسید (ویتامین C) موجود در نوشابهها واکنش داده و مقادیر بسیار کم (ولی در دراز مدت خطرناک) بنزن تولید می شود.
بنزوئیک اسید (BA) یک نگهدارنده ضد میکروبی است که معمولاً در غذاها و نوشیدنیها بهویژه در نوشیدنیهای گازدار استفاده میشود، زیرا قویترین فعالیت ضد باکتریایی خود را در pH 2.5-4.0 نشان میدهد. BA دارای اثرات بازدارنده بر تکثیر باکتری ها و مخمرها است که یکی از دلایل اصلی فساد مواد غذایی است.
اگرچه افزودن BA می تواند عمر مفید نوشیدنی ها را افزایش دهد و از ضررهای تغذیه ای جلوگیری کند، مصرف بیش از حد BA ممکن است باعث اسهال، درد شکم و سایر علائم شود و حتی در فرآیندهای متابولیک میانی بدن اختلال ایجاد کند.
بنابراین، حداکثر غلظت مجاز BA در هر نوع غذا توسط قانون محدود شده است. طبق سازمان غذا و داروی ایالات متحده، محدودیت افزودن BA در انواع کلی غذا به میزان 1000 میلی گرم در کیلوگرم در کیلوگرم حفظ می شود.6).
اسید بنزوئیک دارویی
اسید بنزوئیک به عنوان یک ماده غیر فعال در صنعت داروسازی، به عنوان نگهدارنده ضد میکروبی، ضد قارچ و روان کننده قرص و کپسول استفاده می شود. این ماده در ترکیب با اسید سالیسیلیک، مانند پماد ویتفیلد، برای استفاده به عنوان ضد قارچ برای پای ورزشکاران و کرم حلقوی استفاده شده است. این ماده جزئی از پماد Whitfield است که برای درمان بیماریهای قارچی پوست و مو استفاده میشود.7).
عوارض اسید بنزوئیک
بنزوئیک اسید در شرایط عادی غیر سمی و پایدار است. در حالی که محدودیت های مواجهه شغلی ایجاد نشده است، ممکن است خطری برای سلامتی داشته باشد و بنابراین، شیوه های کار ایمن باید همیشه رعایت شود:
پس از دست زدن، دست ها را کاملا بشویید.
تنها در یک منطقه خوب تهویه شده استفاده شود.
تولید و تجمع گرد و غبار را به حداقل برسانید.
از تماس با پوست، چشم و لباس اجتناب شود.
لباس ها را قبل از استفاده مجدد بشویید.
از تنفس گرد و غبار خودداری کنید.8).
فروش اسید بنزوئیک
برای دریافت اطلاعات بیشتر در مورد خرید اسید بنزوئیک و قیمت اسید بنزوئیک با شماره های 02144182743 و 09026715830 با شرکت آرکا شیمی گستر سپیدار تماس حاصل فرمایید.


نقد و بررسیها
هنوز بررسیای ثبت نشده است.