اتانول چیست و چه کاربردی دارد
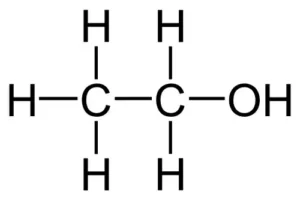
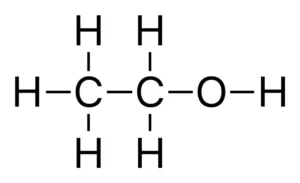
اتانول به عنوان الکل اتیلیک، الکل نوشیدن، الکل دانه، متیل کاربینول، TSDA یا Ethos نیز شناخته می شود. یک ترکیب شیمیایی آلی با فرمول شیمیایی C2H6O است. این یک الکل اولیه و عنصر اصلی موجود در نوشیدنی های الکلی است که در سراسر جهان مصرف می شود.
فرار، قابل اشتعال، شفاف، بی رنگ با بوی شرابی شبیه شراب است. این با آب و بسیاری از حلال های آلی قابل اختلاط است. به این معنی که اتانول در آب حل می شود. طیف وسیعی از کاربردها از جمله به عنوان یک ضد عفونی کننده، پادزهر، یک منبع سوخت و یک حلال است.
فرمول اتانول
- فرمول شیمیایی اتانول: C2H6O / CH3-CH2-OH / C2H5OH
- مترادف: الکل اتیلیک، الکل دانه، متیل کاربینول، TSDA، Ethos، الکل مطلق، الکل نوشیدن، الکل اتیلیک، هیدروکسی اتان
- شماره Cas: 64-17-5
- جرم مولی اتانول: 46.041 g·mol-1
- جرم دقیق: 46.041865 گرم در مول
- نقطه اشتعال: 55 درجه فارنهایت / 12.8 درجه سانتی گراد
- نقطه جوش اتانول: 173.3 درجه فارنهایت / 78.5 درجه سانتی گراد در 760 میلی متر جیوه
- نقطه ذوب: -173.4 درجه فارنهایت / -114.1 درجه سانتیگراد
- فشار بخار: 59.3 میلی متر جیوه در 25 درجه سانتی گراد
- حلالیت در آب: قابل امتزاج
- چگالی اتانول: 0.7893 گرم در مکعب (در 20 درجه سانتی گراد)
این ماده به طور طبیعی در ذرت، ادرار،مدفوع ،خون و عرق، انتشارات ناشی از آتش سوزی، آتشفشان ها، حشرات، تخمیر قندها و همچنین میوه ها وجود دارد. اتانول خوراکی یک محصول جانبی متابولیسم مخمر است که نشان می دهد در اکثر زیستگاه های مخمر وجود دارد و در طول جوانه زنی گیاهان نیز تولید می شود.
تولید اتانول
اتانول و متانول هزاران سال است که تولید میشود و یکی از قدیمیترین فرآیندهای آلی است که بشر از آن استفاده کرده است و مردم در طول تاریخ از خواص آن استفاده میکنند.
از لحاظ تاریخی، از طریق تخمیر که فرآیند تبدیل قندها، مانند گلوکز، تولید میشود:
C6H12O6 → 2 CH3CH2OH + 2 CO2
حجم زیادی از الکل اتانول هنوز از طریق تخمیر تولید می شود و عمدتاً برای استفاده های الکلی و سوختی استفاده می شود. مواد خام را می توان در جایگزینی قندها، از جمله نشاسته و مواد اولیه مبتنی بر قند، مانند دانه ذرت یا نیشکر، یا مواد اولیه سلولزی مانند علف، چوب، بقایای محصول یا ضایعات کشاورزی استفاده کرد.
دی اکسید کربن همچنین می تواند برای جایگزینی قندها یا مواد خام با استفاده از واکنش های الکتروشیمیایی استفاده شود. با این حال، این روش تمایل به تولید مقادیر کمتر این ماده را دارد.
روش دیگر تولید این ماده از طریق هیدراتاسیون اتیلن با کاتالیزور اسیدی در حضور کاتالیزوری مانند اسید فسفریک است:
C2H4 + H2O → CH3CH2OH
این روش معمولاً برای تولید این ماده برای مصارف حلال استفاده می شود. این ماده همچنین از طریق هیدرولیز آنزیمی سلولز، آسیاب مرطوب ذرت و اکسیداسیون متان تولید می شود.
این ماده برای استفاده در طیف وسیعی از صنایع تولید می شود که تقاضا در صنعت سوخت یکی از آنها است، جایی که تغییرات قوانین، تولیدکنندگان سوخت را ملزم به افزایش درصد این ماده در سوخت خود می کند. تولید جهانی اتانول با حدود 52 میلیون تن در سال 2008 بوده که در حال افزایش است.
واکنش ها
واکنش سوختن اتانول بسیار بالا است. با استیل برومید و کلرید به شدت واکنش می دهد و اگر اتانول با پراکسید هیدروژن بسیار غلیظ مخلوط شود، مخلوط های انفجاری می تواند ایجاد شود.
در چندین واکنش آنزیمی از این ماده استفاده می شود که یکی از آنها اکسید شدن اتانول به استالدهید با نیکوتین آمید-آدنین دی نوکلئوتید در حضور کاتالیزور الکل دهیدروژناز است:
اتانول + NAD + → استالدهید + NADH + H +
سایر واکنش ها شامل اسید هیپوکلرو یا کلر برای تشکیل هیپوکلریت اتیل است. این ماده با اسیدهای کربوکسیلیک مانند آمینو یا اسیدهای چرب واکنش می دهد تا اتیل استرها را در حضور یک کاتالیزور اسیدی مانند اسید هیدروفلوئوریک و فسفریک تولید کند.
RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2O
سایر واکنش ها شامل احتراق اتانول تشکیل دهنده CO2 و آب، واکنش با فلزات قلیایی یا بازهای قوی و کم آبی اتانول با یک کاتالیزور اسیدی است.
خطرات و سمیت
اتانول دارای رتبه NFPA 2 است و می تواند باعث ناتوانی موقت و آسیب شود. این ماده به شکل بخار چشم، بینی و گلو را تحریک می کند و تقریباً در تمام شرایط دمایی محیط قابل احتراق است.
مسمومیت با اتانول
وسایل حفاظت فردی باید همیشه هشدار داده شوند تا از تماس احتمالی با پوست و چشم جلوگیری شود. در صورت تماس با پوست، بلافاصله محل آلوده را بشویید. لباس های خیس باید فوراً درآورده و جایگزین شوند.
در صورت نشتی، سعی کنید نشت را تا حداقل 50 متر جدا کنید. نشت باید با استفاده از زمین خشک یا مواد غیر قابل احتراق جذب شود. دسترسی به فاضلاب، زیرزمین و آبراه ها باید مسدود شود. باید از فوم مقاوم در برابر الکل، CO2 یا خاموش کننده های اسپری آب استفاده شود. منابع اشتعال باید حذف شوند تا از آتش سوزی یا آتش سوزی بیشتر جلوگیری شود.
ذخیره سازی و توزیع
اتانول در مخازن ذخیره سازی و/یا بشکه های فولادی ضد زنگ ذخیره می شود و می توان آن را با کشتی های فله یا کامیون های مخزن حمل کرد.
برای اهداف حمل و نقل، این ماده در گروه بسته بندی II و کلاس خطر 3 طبقه بندی می شود، زیرا دارای نقطه اشتعال 14 درجه سانتیگراد است و بسیار قابل اشتعال است. باید در مکانی خنک، خشک و دارای تهویه مناسب و عاری از هرگونه خطر آتش سوزی نگهداری شود. وزن مخصوص آن 0.789 است.
کاربرد اتانول
- مصارف صنعتی: استفاده اولیه از الکل اتانول خوراکی در تولید مشروبات الکلی است. سایر مصارف تولیدی شامل تولید استالدئید، اتیل کلرید، اتیل استات، اتیلن دی بروماید، اسید استیک، گلیکول اترها، اتیلامین ها و همچنین در مواد منفجره، رنگ ها، مواد شوینده، پرکننده ها، روان کننده ها، لاک ها، افزودنی ها، پوشش ها، عطرها، مواد غذایی، عصاره طعم دهنده ها، بنزین و مواد دارویی.
کاربردهای دارویی اتانول به عنوان یک ضد عفونی کننده در دستمال مرطوب و اسپری ضد باکتری است. همچنین گاهی اوقات به عنوان پادزهر مسمومیت با متانول و به عنوان نوروتوکسین، عامل تراتوژن و متابولیت انسانی استفاده می شود.
این ماده می تواند درد مزمن را برای بیماران سرطانی غیرقابل جراحی از طریق نورولیز اعصاب تسکین دهد.
یکی دیگر از کاربردهای اولیه این ماده به عنوان یک افزودنی سوخت مشعل پاک کننده موتور است. اکثر بنزین تولید شده در ایالات متحده حاوی 10٪ این ماده است که سوخت را اکسیژن می کند و آلودگی آن را کاهش می دهد.
- موارد استفاده به عنوان حلال: اتانول کاربردهای زیادی به عنوان حلال دارد از جمله برای رزین ها، اسیدهای چرب، هیدروکربن ها، چربی ها، روغن ها و موم ها. همچنین در محصولات مراقبت شخصی، محصولات مراقبت از هوا، رنگ ها و نشانگرها وجود دارد. ساختار این ماده امکان حل شدن در ترکیبات قطبی مانند آب، غیر قطبی و آبدوست مانند هگزان و آبگریز را فراهم می کند.
اتانول به دلیل سمیت کم و قابلیت های غیر قطبی به عنوان یک حلال دارویی نیز استفاده می شود. در داروهای مسکن و داروهای سرفه و سرماخوردگی دیده می شود.
تشخیص اتانول از متانول
به تازگی میزان مرگ و میر در ایران با مصرف متانول بالا رفته است. مصرف متانول به میزان بسیار کم هم می تواند کشنده باشد. حتی مصرف متانول می تواند بعد از سه تا چهار روز بعد از مصرف به مرگ منجر شود.
مطلبی به عنوان روش خانگی تشخیص اتانول از متانول وجود ندارد و نمیتوان به قطعیت در مورد تشخیص این دو ماده خارج از محیط آزمایشگاهی نظری ارائه داد. با این حال برای انجام تست تشخیص آنها، مقداری از هر کدام یا ترکیب هر دو را در یک ظرف قرار دهید.
به آنها شعله بدمید و مشاهده کنید که آیا شعله بهصورت آبی و براق می سوزد یا آبی کثیف و دودی شکل. تفاوت سوختن این دو ماده در رنگ آنها است.
سوختن اتانول شعله آبی و براق را به همراه دارد، زیرا این ماده با دمای بالا و در حضور هوا بهصورت کامل سوخته و شعله آبی را تشکیل میدهد. اما متانول با دمای پایینتر و با تشکیل شعله آبی کثیف و دودی میسوزد.
تشخیص اتانول از متانول با جوش شیرین
برای تشخیص اتانول از متانول با جوش شیرین محلول را با جوش شیرین مخلوط میکنیم، اگر رسوب زرد رنگ تشکیل شد، محلول اتانول است و اگر رسوب تشکیل نشد، محلول متانول بوده است.
تشخیص اتانول از متانول با سیب زمینی
برای تشخیص اتانول از متانول با سیب زمینی، سیب زمینی را داخل محلول قرار می دهیم. اگر سیب زمینی به رنگ سبز در آمد اتانول و در صورتی که به رنگ صورتی تغییر رنگ داد محلول متانول است.
این چند روش بسیار ساده هستند، اما بههیچ عنوان روش قطعی و دقیق در نظر گرفته نمی شوند، زیرا مواد دیگر موجود در محلول ها نیز ممکن است شعله آبی و براق تشکیل دهند؛ بنابراین، برای اطمینان بیشتر و تشخیص بهتر، استفاده از روشهای آزمایشگاهی پیشنهاد میشود.
کاربردهای تجاری اتانول
خرید اتانول به دلیل خاصیت پاک کنندگی در بسیاری از محصولات آرایشی، زیبایی و مراقبت شخصی، ژل های ضد باکتری و ضد عفونی کننده ها یافت می شود و به جدا شدن اسپری ها در هوا و جلوگیری از شکافتن لوسیون ها و ژل ها کمک می کند.
همچنین در رنگ ها، لاک ها، روغن ها، عصاره وانیل، سوخت، نوشیدنی های الکلی، ضد یخ ها، جوهرها، چسب ها نیز وجود دارد.
اتانول قطبی است یا ناقطبی
الكل ها همگی دارای گروه عاملی هیدروكسید یا OH هستند. گروه هیدروكسید OH یك گروه قطبی می باشد زیرا الكترونگاتیوی ئیدروژن و كربن بیش از 4/0 می باشد.
اصل كلی كه در حلالیت وجود دارد این است كه مواد قطبی در حلال های قطبی حل می شوند و مواد ناقطبی در حلال های ناقطبی حل می شوند. الكل ها نیز مانند آب دارای ئیدروژن متصل به اكسیژن هستند و بنابراین توانایی برقراری پیوند هیدروژنی بین مولكولهای خود و نیز بین خود و آب را دارند.
اطلاعات تماس
- تهران چیتگر خیابان سروناز خیابان گودرزی کوچه هجدهم پلاک 40
- 02144182743
- 02144194673
- 09026715830
- info@arkachem.ir